Nhận biết một số chất khí: Tổng hợp Lý thuyết và Một số dạng bài tập
Trong chương trình hóa học 12, các em cần nắm chắc kiến thức về một số chất khí bằng phương pháp hóa học. Trong bài viết chi tiết dưới đây, Tip.edu.vn sẽ giúp các bạn tìm hiểu cụ thể về chủ đề nhận biết một số chất khí và các bài tập liên quan.
Nhận biết chất khí là gì?
Các nguyên tắc khi giải bài tập nhận biết các chất khí
- Để nhận biết và phân biệt các hóa chất, chúng ta cần dựa vào phản ứng đặc trưng cũng như hiện tượng dễ nhận biết: như có kết tủa tạo thành sau phản ứng, sự thay đổi màu sắc của dung dịch hoặc có mùi khai, hoặc sự hiện diện của bọt khí. Bên cạnh đó, chúng ta cũng có thể sử dụng một số tính chất vật lý như tính hòa tan, dễ phân hủy hoặc mùi đặc trưng, v.v.
- Để nhận biết một số chất khí, phản ứng hoá học đã chọn phải được đặc trưng bởi những dấu hiệu đơn giản và rõ ràng. Trừ trường hợp đặc biệt, để nhận biết được n hoá chất cần tiến hành (n – 1) thí nghiệm.
- Thuốc thử chính là những chất được lựa chọn để phát hiện một số khí nhất định.
Các bước tiến hành dò khí
- Bước 1: Chiết (chiết mẫu thử) hóa chất cần xác định vào các ống nghiệm và (đánh số thứ tự)
- Bước 2: Lựa chọn thuốc thử thích hợp (tùy theo yêu cầu của đề: thuốc thử tùy chọn, hạn chế hoặc không sử dụng thuốc thử khác).
- Bước 3: Cho vào ống nghiệm ghi các hiện tượng xảy ra và rút ra kết luận.
- Bước 4: Viết phương trình hóa học minh họa.
Các dạng bài tập nhận biết một số chất khí
- Hình thức 1: Nhận biết các chất hóa học (rắn, lỏng, khí) riêng biệt.
- Dạng 2: Nhận biết các chất đựng trong các lọ riêng biệt không nhãn.
- Dạng 3: Cần xác định sự có mặt của các chất (hoặc ion) trong cùng một dung dịch.
- Ghi chú: Tùy theo yêu cầu của bài tập, ở mỗi dạng bài có thể gặp một trong các trường hợp sau:
- Nhận dạng bằng thuốc thử tự do (nhưng không giới hạn thuốc thử).
- Hạn chế dùng thuốc thử (sử dụng 1 thuốc thử và không sử dụng hóa chất khác).
- Nhận thấy không được dùng thuốc thử bên ngoài (Với yêu cầu này ta lập một bảng sẽ giúp vừa nhận biết được hóa chất, vừa lấy chất đó làm thuốc thử).
Tìm hiểu và nhận biết hóa chất đối với chất khí
CO. khí ga
- Thuốc thử: Dung dịch (PdCl_ {2} )
- Hiện tượng: dung dịch sẫm màu, có khí thoát ra
- Phương trình phản ứng:
(CO + H_ {2} O + PdCl_ {2} mũi tên phải 2HCl + CO_ {2} + Pd )
Khí Co2} )
- Thuốc thử: Dùng nước vôi trong
- Hiện tượng xảy ra làm đục nước vôi trong, sau đó dung dịch trở nên trong suốt.
- Phương trình phản ứng:
(CO_ {2} + Ca (OH) _ {2} rightarrow CaCO_ {3} + H_ {2} O )
(CaCO_ {3} + H_ {2} O + CO_ {2} rightarrow Ca (HCO_ {3}) _ {2} )
Khí (SO_ {2} )
- Khí (SO_ {2} ) thường có mùi hắc, khó ngửi và làm phai màu hoa hồng.
- Thuốc thử: Dùng dung dịch brom hoặc dung dịch thuốc tím.
- Hiện tượng: Dung dịch nước Brôm mất màu hoặc dung dịch thuốc tím.
- Phương trình phản ứng:
(Br_ {2} + 2H_ {2} O + SO_ {2} rightarrow H_ {2} SO_ {4} + 2HBr )
(5SO_ {2} + 2KMnO_ {4} + 2H_ {2} O rightarrow 2H_ {2} SO_ {4} + 2MnSO_ {4} + K_ {2} SO_ {4} )
Khí (SO_ {3} )
- Thuốc thử: Dung dịch (BaCl_ {2} )
- Hiện tượng: Xuất hiện kết tủa trắng.
- Phương trình phản ứng:
(BaCl_ {2} + H_ {2} O + SO_ {3} rightarrow 2HCl + BaSO_ {4} )
Khí (NH_ {3} )
- Khí (NH_ {3} ) có mùi hắc, làm xanh quỳ ẩm.
- Thuốc thử: Axit HCl đặc
- Hiện tượng: Xuất hiện khói trắng
- Phương trình phản ứng:
(HCl + NH_ {3} rightarrow NH_ {4} Cl )
Khí clo
- Thuốc thử: Dùng dung dịch KI + Hồ tinh bột
- Hiện tượng: Dung dịch chuyển từ màu trắng sang màu xanh lam.
- Phương trình phản ứng:
(Cl_ {2} + KI mũi tên phải 2KCl + I_ {2} )
Khí (H_ {2} S )
- Khí (H_ {2} S ) có mùi trứng thối.
- Thuốc thử: Sử dụng dung dịch (Pb (NO_ {3}) _ {2} )
- Hiện tượng: Sản phẩm tạo thành là PbS kết tủa màu đen.
- Phương trình phản ứng:
(Pb (NO_ {3}) _ {2} + H_ {2} S rightarrow PbS + 2HNO_ {3} )
Khí HCl
- Khí HCl làm giấy quỳ ẩm chuyển sang màu đỏ.
- Thuốc thử: Dung dịch (AgNO_ {3} )
- Hiện tượng: Sản phẩm tạo thành AgCl kết tủa trắng.
- Phương trình phản ứng:
(AgNO_ {3} + HCl ngay AgCl + HNO_ {3} )
Khí NO (không màu)
- Thuốc thử: Không khí
- Hiện tượng: nâu đỏ
- Phương trình phản ứng:
(2NO + O_ {2} rightarrow 2NO_ {2} )
Khí (NO_ {2} )
- Thuốc thử: quỳ tím ẩm
- Hiện tượng: Làm quỳ tím hóa đỏ.
- Hoặc để nguội thì màu nâu đỏ nhạt dần, sau đó mất màu, khi nguội lại xuất hiện màu đỏ nâu.
- Phương trình phản ứng:
(2NO_ {2} rightarrow N_ {2} O_ {4} )
Khí (O_ {3} ) (ôzôn)
- Thuốc thử: Dung dịch KI và hồ tinh bột
- Hiện tượng: tạo thành dung dịch xanh tím.
- Phương trình phản ứng:
(O_ {3} + 2KI + H_ {2} O mũi tên phải KOH + I_ {2} + O_ {2} )
Khí (O_ {2} )
- Thuốc thử: Than đỏ
- Hiện tượng: Than cháy.
- Phương trình phản ứng:
(C + O_ {2} rightarrow CO_ {2} )
Khí (N_ {2} )
- Thuốc thử: Red Match
- Hiện tượng: Khí (N_ {2} ) làm cho que diêm tắt.
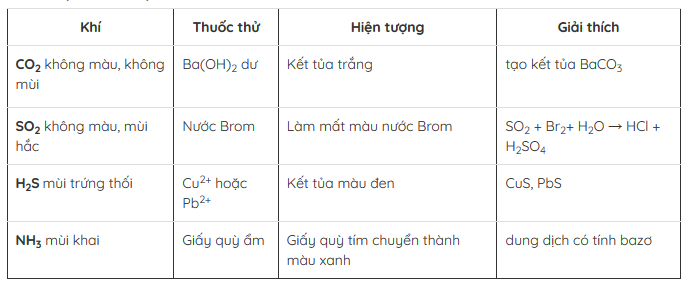
Một số bài tập về nhận biết chất khí
Loại 1: Bài tập không hạn chế về thuốc thử hoặc phương pháp sử dụng
Ví dụ 1: Có hai bể riêng biệt cho khí (CO_ {2} ) và (SO_ {2} ). Trình bày cách nhận biết từng chất khí. Viết các phương trình hóa học.
Dung dịch:
Lần lượt cho hai khí đi qua dung dịch nước brom nếu khí làm mất màu dung dịch nước brom là (SO_ {2} ).
Khí còn lại dẫn vào bình đựng nước vôi trong, nếu thấy kết tủa làm đục nước vôi trong là (CO_ {2} )
Phương trình phản ứng:
(SO_ {2} + Br_ {2} + 2H_ {2} O rightarrow 2HBr + H_ {2} SO_ {4} )
(CO_ {2} + Ca (OH) _ {2} rightarrow CaCO_ {3} + H_ {2} O )
Loại 2: Thuốc thử hoặc phương pháp hạn chế sử dụng
Đây là dạng bài tập yêu cầu học sinh giải quyết vấn đề của bài tập trong một điều kiện nhất định.
Ví dụ 2: Có các lọ thuốc thử không nhãn, mỗi lọ đựng một trong các dung dịch không màu sau: (Na_ {2} SO_ {4}, Na_ {2} S, Na_ {2} CO_ {3}, Na_ {3} PO_ {4}, Na_ {2} SO_ {3} ). Chỉ dùng thuốc thử là nhỏ trực tiếp dung dịch (H_ {2} SO_ {4} ) loãng vào từng dung dịch thì có thể nhận biết được những dung dịch nào?
Dung dịch:
Cho dung dịch (H_ {2} SO_ {4} ) loãng vào 5 lọ lần lượt chứa 5 dung dịch:
- Lọ nào chứa chất khí không màu, không mùi là (Na_ {2} CO_ {3} )
(Na_ {2} CO_ {3} + H_ {2} SO_ {4} rightarrow Na_ {2} SO_ {4} + H_ {2} O + CO_ {2} )
- Cái chai có mùi trứng thối là (Na_ {2} S )
(Na_ {2} S + H_ {2} SO_ {4} rightarrow Na_ {2} SO_ {4} + H_ {2} S )
- Lọ nào có khí không màu, mùi hắc là (Na_ {2} SO_ {3} )
(Na_ {2} SO_ {3} + H_ {2} SO_ {4} rightarrow Na_ {2} SO_ {4} + H_ {2} O + SO_ {2} )
- 2 chai còn lại không có biểu hiện gì
( Rightarrow ) Xác định 3 giải pháp là (Na_ {2} CO_ {3}, Na_ {2} S, Na_ {2} SO_ {3} )
Như vậy là Tip.edu.vn đã cùng các bạn tìm hiểu về kiến thức nhận biết một số chất khí. Hi vọng những thông tin trong bài sẽ giúp ích cho các bạn trong quá trình nghiên cứu cũng như học tập chuyên đề nhận biết một số chất khí. Chúc may mắn với các nghiên cứu của bạn!.
Xem thêm nhiều bài viết hay về Hỏi Đáp Hóa Học
